本文目录导读:
锰(Mn)是一种重要的过渡金属元素,在化学、材料科学、生物学等领域具有广泛的应用,由于其丰富的电子排布,锰原子在形成化合物时,其杂化类型多样,表现出丰富的化学性质,本文将详细介绍锰的杂化类型,包括其成因、种类以及在不同化合物中的应用。
锰的基本电子排布
在探讨锰的杂化类型之前,我们先了解锰原子的电子排布,锰的原子序数为25,其基态电子排布为[Ar] 3d^5 4s^2,在化学反应中,锰可以失去两个电子形成Mn2+离子,此时其电子排布变为[Ar] 3d^5,呈现出较缺电子的状态,易于接受电子形成化学键。
锰的杂化类型成因
杂化是指原子在分子形成过程中,为了满足其价电子的成键需求,重新组合其价电子的行为,对于锰而言,由于其d轨道存在未被完全填满的电子,因此在与其他原子形成化学键时,这些电子会进行重新排列和组合,形成不同的杂化轨道,这些杂化轨道使得锰能够与其他原子形成稳定的化学键,从而构成各种化合物。
锰的主要杂化类型
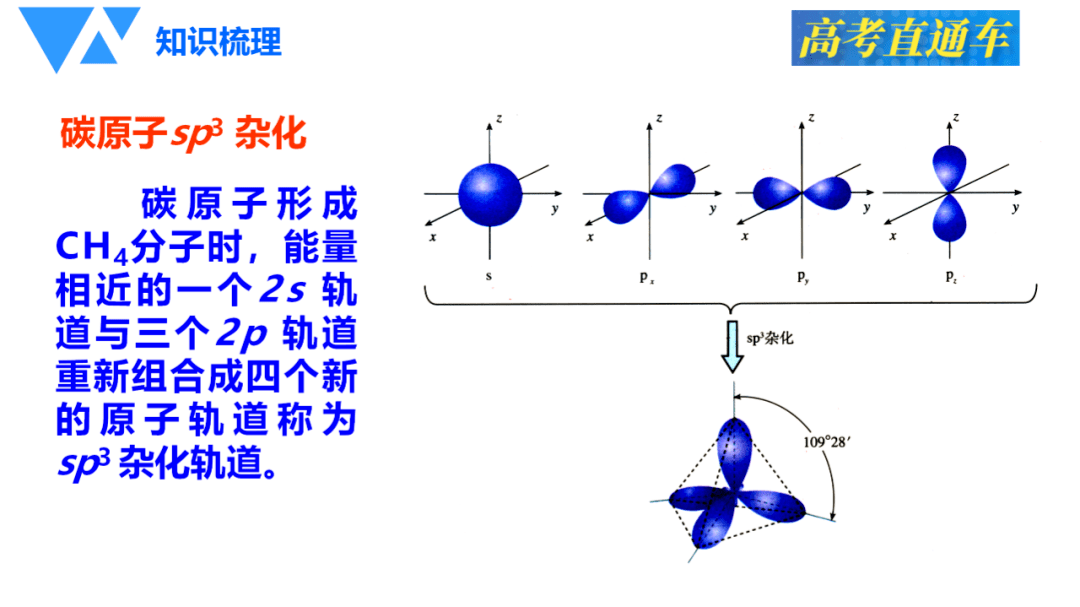
1、sp3杂化:sp3杂化是指s轨道和三个p轨道发生杂化,形成四个等价的杂化轨道,在锰形成的某些化合物中,如Mn(CO)5-等配合物中,存在sp3杂化。
2、d2sp3杂化:这是一种涉及d轨道和s、p轨道的杂化类型,在形成一些复杂的离子或配合物时,如Mn2+与配体形成的配合物中,d2sp3杂化较为常见,这种杂化类型使得锰能够与其他原子形成稳定的配位键。
3、sp2杂化:在某些情况下,锰的s轨道和两个p轨道发生杂化,形成三个等价的杂化轨道,这种杂化类型在一些小分子或离子中较为常见。
不同杂化类型在化合物中的应用
1、sp3杂化:在Mn(CO)5-等配合物中,中心锰原子的sp3杂化使得该配合物具有四面体构型,表现出较高的稳定性。
2、d2sp3杂化:在Mn2+与配体形成的配合物中,d2sp3杂化使得配合物具有高度的稳定性,并且呈现出多样的配位数和构型,这种杂化类型的化合物在材料科学、生物学等领域具有广泛的应用。
3、sp2杂化:在一些小分子或离子中,如MnX3(X为卤素)中,锰原子的sp2杂化使得这些化合物具有平面三角形构型。
锰的杂化类型多样,包括sp3、d2sp3和sp2等,这些杂化类型使得锰在形成化合物时具有高度的灵活性,表现出丰富的化学性质,深入研究锰的杂化类型对于理解其在化学、材料科学、生物学等领域的应用具有重要意义。
展望
尽管关于锰的杂化类型已经取得了一定的研究成果,但仍有许多问题需要进一步探讨,不同杂化类型的形成条件和机制、锰的杂化类型与其化合物性质的关系等,未来的研究将更加注重理论和实验的相结合,以揭示锰的杂化类型的更多奥秘,随着计算化学的发展,利用计算机模拟来预测和解释锰的杂化类型及其化合物性质将成为一种重要手段。


 京公网安备11000000000001号
京公网安备11000000000001号 京ICP备11000001号
京ICP备11000001号
还没有评论,来说两句吧...